Ver
Insuficiencia hepática: No se requiere ajuste de dosis para pacientes con deterioro hepático.
Población pediátrica: La seguridad y eficacia de la pregabalina en nińos menores de 12 ańos y en adolescentes (de 12 a 17 ańos) no han sido establecidas. Los datos disponibles actualmente se describen en las secciones 4.8 y 5.2, pero no se puede hacer ninguna recomendación sobre la posología.
Adultos mayores: Los pacientes ancianos pueden requerir una reducción de dosis de pregabalina debido a una disminución de la función renal.
Método de administración: Prexel CR debe tomarse directamente después de una comida nocturna. Prexel CR comprimido debe tragarse entero y no debe partirse, triturarse ni masticarse. El comprimido no debe romperse porque esto podría afectar las características de liberación prolongada. Prexel CR es solo para uso oral.
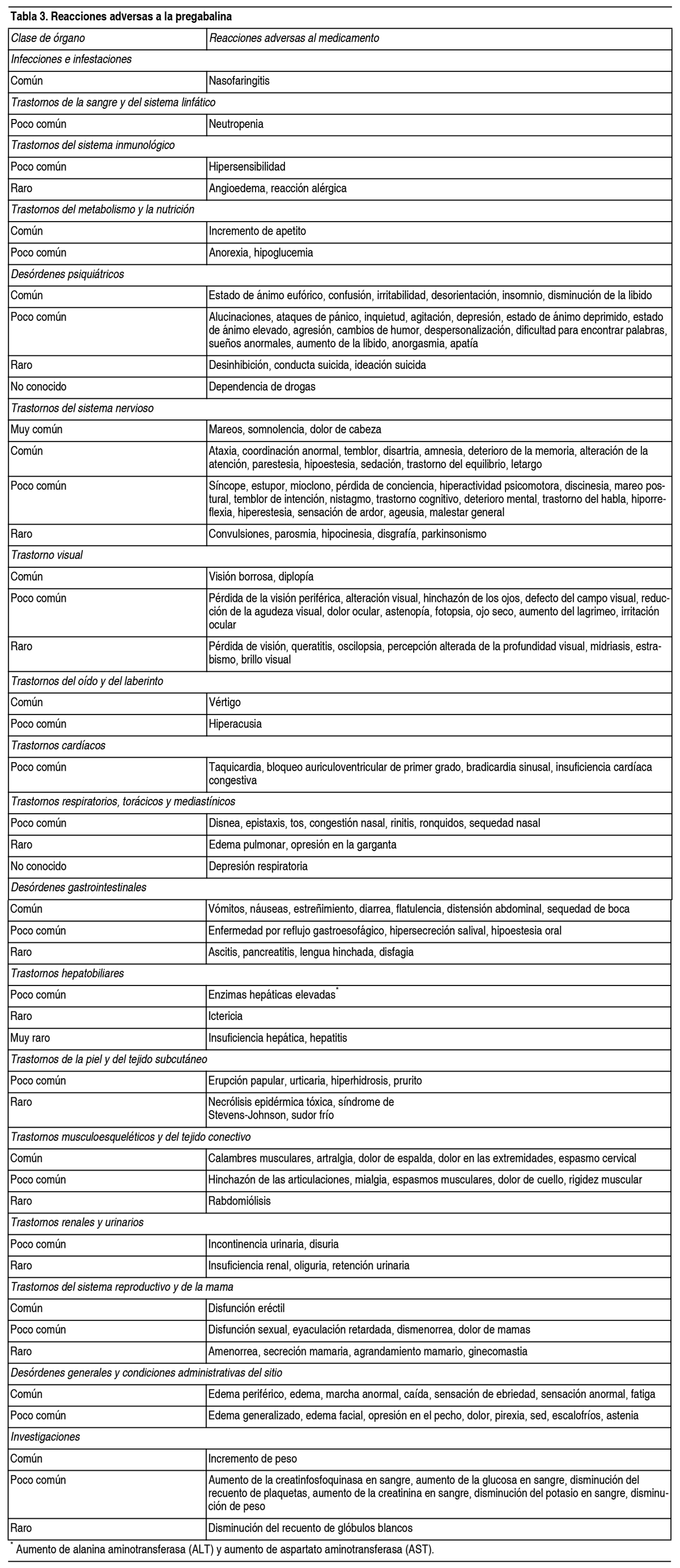
Efectos Colaterales: El programa clínico de pregabalina incluyó a más de 8900 pacientes expuestos a pregabalina, de los cuales más de 5600 participaron en ensayos controlados con placebo a doble ciego. Las reacciones adversas más comúnmente reportadas fueron mareos y somnolencia. Las reacciones adversas generalmente fueron de leve a moderada intensidad. En todos los estudios controlados, la tasa de discontinuación debido a reacciones adversas fue del 12 % para pacientes que recibieron pregabalina y del 5 % para pacientes que recibieron placebo. Las reacciones adversas más comunes que resultaron en la interrupción del tratamiento con pregabalina fueron mareos y somnolencia. En la Tabla 3 a continuación, se listan todas las reacciones adversas que ocurrieron con una incidencia mayor que el placebo y en más de 1 paciente, clasificadas por frecuencia (muy común [≥1/10], común [≥1/100 a <1/10], poco común [≥000 a <1/100], raro [≥1/10 000 a <1/1000], muy raro [<1/10 000]), no conocido [no se puede estimar a partir de los datos disponibles]). Dentro de cada grupo de frecuencia, se presentan los efectos no deseados en orden de gravedad decreciente. Las reacciones adversas enumeradas también pueden estar asociadas con la enfermedad subyacente y/o productos medicinales concomitantes. En el tratamiento del dolor neuropático central debido a lesión de la médula espinal, se observó un aumento en la incidencia de reacciones adversas en general, reacciones adversas del sistema nervioso central y especialmente somnolencia. Reacciones adicionales reportadas en la experiencia poscomercialización están incluidas en cursiva en la lista a continuación.
Después de la discontinuación del tratamiento a corto y largo plazo con pregabalina, se han observado síntomas de abstinencia en algunos pacientes. Se han mencionado las siguientes reacciones: Insomnio, dolor de cabeza, náuseas, ansiedad, diarrea, síndrome gripal, convulsiones, nerviosismo, depresión, dolor, hiperhidrosis y mareos. Estos síntomas pueden indicar dependencia a la droga. El paciente debe ser informado sobre esto al inicio del tratamiento. En cuanto a la discontinuación del tratamiento a largo plazo con pregabalina, los datos sugieren que la incidencia y gravedad de los síntomas de abstinencia pueden estar relacionados con la dosis. Población pediátrica: El perfil de seguridad de la pregabalina observado en 5 estudios pediátricos en pacientes con crisis parciales con o sin generalización secundaria (estudio de eficacia y seguridad de 12 semanas en pacientes de 4 a 16 ańos, n=295; estudio de eficacia y seguridad de 14 días en pacientes de 1 mes a menos de 4 ańos, n=175; estudio farmacocinético y de tolerabilidad, n=65; y 2 estudios de seguimiento de seguridad abiertos de 1 ańo, n=54 y n=431) fue similar al observado en los estudios en adultos con epilepsia. Los eventos adversos más comunes observados en el estudio de 12 semanas con tratamiento de pregabalina fueron somnolencia, fiebre, infección del tracto respiratorio superior, aumento del apetito, aumento de peso y nasofaringitis. Los eventos adversos más comunes observados en el estudio de 14 días con tratamiento de pregabalina fueron somnolencia, infección del tracto respiratorio superior y fiebre. Notificación de reacciones adversas sospechosas: La notificación de reacciones adversas sospechosas después de la autorización del producto medicinal es importante. Permite continuar monitoreando el balance beneficio/riesgo del producto medicinal. Se solicita a los profesionales de la salud que notifiquen cualquier reacción adversa sospechada a través del sistema nacional de notificación.
Contraindicaciones: Hipersensibilidad a la sustancia activa o a cualquiera de los excipientes.
Advertencias: Pacientes diabéticos: De acuerdo con la práctica clínica actual, algunos pacientes diabéticos que aumentan de peso durante el tratamiento con pregabalina pueden necesitar ajustar los productos medicinales hipoglucémicos. Reacciones de hipersensibilidad: Se han reportado reacciones de hipersensibilidad, incluyendo casos de angioedema, en la experiencia posterior a la comercialización. La pregabalina debe suspenderse de inmediato si aparecen síntomas de angioedema, como hinchazón facial, perioral o de las vías respiratorias superiores. Reacciones adversas cutáneas graves (RACS): Se han reportado RACS, incluyendo el síndrome de Stevens-Johnson (SJS) y la necrólisis epidérmica tóxica (TEN), que pueden ser potencialmente mortales, en asociación con el tratamiento con pregabalina. En el momento de la prescripción, se debe informar a los pacientes sobre los signos y síntomas y se debe monitorear de cerca para detectar reacciones en la piel. Si aparecen signos y síntomas sugestivos de estas reacciones, se debe suspender la pregabalina inmediatamente y considerar un tratamiento alternativo (según corresponda). Mareos, somnolencia, pérdida de conciencia, confusión y deterioro mental: El tratamiento con pregabalina se ha asociado con mareos y somnolencia, lo cual podría aumentar la incidencia de lesiones accidentales (caídas) en la población anciana. También se han reportado casos de pérdida de conciencia, confusión y deterioro mental en la experiencia posterior a la comercialización. Por lo tanto, se recomienda a los pacientes que tengan precaución hasta familiarizarse con los posibles efectos del producto medicinal. Efectos relacionados con la visión: En ensayos controlados, una proporción más alta de pacientes tratados con pregabalina reportó visión borrosa en comparación con los pacientes tratados con placebo, lo cual se resolvió en la mayoría de los casos con la dosificación continua. En los estudios clínicos donde se realizaron pruebas oftalmológicas, la incidencia de reducción de agudeza visual y cambios en el campo visual fue mayor en los pacientes tratados con pregabalina que en los tratados con placebo; la incidencia de cambios fundoscópicos fue mayor en los pacientes tratados con placebo. En la experiencia posterior a la comercialización, también se han reportado reacciones adversas visuales, incluyendo pérdida de visión, visión borrosa u otros cambios en la agudeza visual, muchos de los cuales fueron transitorios. La interrupción de la pregabalina puede resultar en la resolución o mejoría de estos síntomas visuales. Insuficiencia renal: Se han reportado casos de insuficiencia renal y, en algunos casos, la interrupción de la pregabalina mostró reversibilidad de esta reacción adversa. Insuficiencia cardíaca congestiva: Se han reportado casos de insuficiencia cardíaca congestiva en algunos pacientes que reciben pregabalina. Estas reacciones se observan principalmente en pacientes ancianos con compromiso cardiovascular durante el tratamiento con pregabalina para una indicación neuropática. La pregabalina debe usarse con precaución en estos pacientes. La interrupción de la pregabalina puede resolver la reacción. Tratamiento del dolor neuropático central debido a lesión de la médula espinal: En el tratamiento del dolor neuropático central debido a lesión de la médula espinal, se observó un aumento en la incidencia de reacciones adversas en general, reacciones adversas del sistema nervioso central y especialmente somnolencia. Esto puede atribuirse a un efecto aditivo debido a medicamentos concomitantes (por ejemplo, agentes antiespásticos) necesarios para esta condición. Esto debe tenerse en cuenta al prescribir pregabalina en esta condición. Depresión respiratoria: Se han reportado casos de depresión respiratoria severa relacionada con el uso de pregabalina. Los pacientes con función respiratoria comprometida, enfermedad respiratoria o neurológica, deterioro renal, uso concomitante de depresores del sistema nervioso central y pacientes ancianos pueden estar en mayor riesgo de experimentar esta reacción adversa severa. Puede ser necesario ajustar la dosis en estos pacientes. Ideación suicida y comportamiento suicida: Se han reportado ideación suicida y comportamiento suicida en pacientes tratados con agentes antiepilépticos en varias indicaciones. Un meta análisis de estudios aleatorizados controlados con placebo de medicamentos antiepilépticos también ha mostrado un pequeńo aumento en el riesgo de ideación y comportamiento suicida. El mecanismo de este riesgo no se conoce. Se han observado casos de ideación y comportamiento suicida en pacientes tratados con pregabalina en la experiencia posterior a la comercialización. Un estudio epidemiológico que utilizaba un diseńo de estudio autocontrolado (comparando períodos de tratamiento con períodos sin tratamiento dentro de un individuo) mostró evidencia de un aumento en el riesgo de inicio de comportamiento suicida y muerte por suicidio en pacientes tratados con pregabalina. Se recomienda a los pacientes (y cuidadores de pacientes) que busquen asesoramiento médico si aparecen signos de ideación o comportamiento suicida. Los pacientes deben ser monitoreados para detectar signos de ideación y comportamientos suicidas y se debe considerar un tratamiento adecuado. Se debe considerar la interrupción del tratamiento con pregabalina en caso de ideación y comportamiento suicida. Función reducida del tracto gastrointestinal inferior: Existen informes posteriores a la comercialización de eventos relacionados con la función reducida del tracto gastrointestinal inferior (por ejemplo, obstrucción intestinal, íleo paralítico, estreńimiento) cuando la pregabalina se administró junto con medicamentos que tienen el potencial de producir estreńimiento, como los analgésicos opioides. Cuando se utilicen pregabalina y opioides en combinación, se pueden considerar medidas para prevenir el estreńimiento (especialmente en pacientes mujeres y ancianos). Uso concomitante con opioides: Se recomienda precaución al prescribir pregabalina de forma concomitante con opioides debido al riesgo de depresión del sistema nervioso central. En un estudio de caso-control de usuarios de opioides, los pacientes que tomaron pregabalina junto con un opioides tuvieron un mayor riesgo de muerte relacionada con opioides en comparación con el uso de opioides solo (odds ratio ajustado [ORa], 1.68 [IC del 95 %, 1.19-2.36]). Este aumento de riesgo se observó en dosis bajas de pregabalina (≤ 300 mg, ORa 1.52 [IC del 95 %, 1.04-2.22]) y hubo una tendencia a un mayor riesgo en dosis altas de pregabalina (>300 mg, ORa 2.51 [IC del 95 %, 1.24-5.06]). Uso indebido, potencial de abuso o dependencia: La pregabalina puede causar dependencia a la droga, lo cual puede ocurrir a dosis terapéuticas. Se han reportado casos de uso indebido, abuso y dependencia. Los pacientes con antecedentes de abuso de sustancias pueden tener un mayor riesgo de uso indebido, abuso y dependencia de la pregabalina, por lo que debe usarse con precaución en tales pacientes. Antes de prescribir pregabalina, se debe evaluar cuidadosamente el riesgo de uso indebido, abuso o dependencia del paciente. Los pacientes tratados con pregabalina deben ser monitoreados por síntomas de uso indebido, abuso o dependencia de pregabalina, como desarrollo de tolerancia, escalada de dosis y comportamiento de búsqueda de drogas. Síntomas de abstinencia: Después de la interrupción del tratamiento a corto y largo plazo con pregabalina, se han observado síntomas de abstinencia. Se han reportado los siguientes síntomas: Insomnio, dolor de cabeza, náuseas, ansiedad, diarrea, síndrome gripal, nerviosismo, depresión, dolor, convulsión, hiperhidrosis y mareos. La aparición de síntomas de abstinencia después de la interrupción de la pregabalina puede indicar dependencia de la droga. Se debe informar al paciente sobre esto al inicio del tratamiento. Si se considera la interrupción de la pregabalina, se recomienda hacerlo gradualmente durante un mínimo de 1 semana independientemente de la indicación. Convulsiones, incluyendo estado epiléptico y convulsiones tónico-clónicas generalizadas, pueden ocurrir durante el uso de pregabalina o poco después de interrumpir la pregabalina. Encefalopatía: Se han reportado casos de encefalopatía, principalmente en pacientes con condiciones subyacentes que pueden precipitar encefalopatía. Mujeres en edad fértil/anticoncepción: El uso de pregabalina en el primer trimestre del embarazo puede causar defectos congénitos graves en el feto. La pregabalina no debe usarse durante el embarazo a menos que el beneficio para la madre claramente supere el riesgo potencial para el feto. Las mujeres en edad fértil deben usar anticonceptivos efectivos durante el tratamiento.
Precauciones: Mujeres en edad fértil/anticoncepción: Las mujeres en edad fértil deben usar anticoncepción efectiva durante el tratamiento. Embarazo: Los estudios en animales han mostrado toxicidad reproductiva. Se ha demostrado que la pregabalina atraviesa la placenta en ratas. Es posible que la pregabalina cruce la placenta humana. Malformaciones congénitas mayores: Datos de un estudio observacional nórdico de más de 2700 embarazos expuestos a pregabalina en el primer trimestre mostraron una mayor prevalencia de malformaciones congénitas mayores (MCM) entre la población pediátrica (nacidos vivos o mortinatos) expuesta a pregabalina en comparación con la población no expuesta (5.9 % vs. 4.1 %). El riesgo de MCM entre la población pediátrica expuesta a pregabalina en el primer trimestre fue ligeramente mayor en comparación con la población no expuesta (razón de prevalencia ajustada y IC del 95 %: 1.14 [0.96-1.35]), y en comparación con la población expuesta a lamotrigina (1.29 [1.01-1.65]) o duloxetina (1.39 [1.07-1.82]). Los análisis sobre malformaciones específicas mostraron mayores riesgos de malformaciones del sistema nervioso, el ojo, fisuras orofaciales, malformaciones urinarias y malformaciones genitales, pero los números fueron pequeńos y las estimaciones imprecisas. Pregabalina no debe ser utilizada durante el embarazo a menos que sea claramente necesario (si el beneficio para la madre claramente supera el riesgo potencial para el feto). Lactancia materna: La pregabalina se excreta en la leche humana. El efecto de la pregabalina en recién nacidos/bebés es desconocido. Debe tomarse una decisión sobre si suspender la lactancia materna o discontinuar la terapia con pregabalina, considerando el beneficio de la lactancia para el nińo y el beneficio de la terapia para la mujer. Fertilidad: No hay datos clínicos sobre los efectos de la pregabalina en la fertilidad femenina. En un ensayo clínico para evaluar el efecto de la pregabalina sobre la motilidad espermática, sujetos varones sanos fueron expuestos a pregabalina a una dosis de 600 mg/día. Después de 3 meses de tratamiento, no hubo efectos sobre la motilidad espermática. Un estudio de fertilidad en ratas hembra ha mostrado efectos adversos reproductivos. Los estudios de fertilidad en ratas macho han mostrado efectos adversos reproductivos y del desarrollo. La relevancia clínica de estos hallazgos es desconocida. Efectos sobre la capacidad para conducir y utilizar máquinas: La pregabalina puede tener una influencia leve o moderada sobre la capacidad para conducir y utilizar máquinas. Prexel CR puede causar mareos y somnolencia y, por lo tanto, puede influir en la capacidad para conducir o utilizar máquinas. Se recomienda a los pacientes no conducir, operar maquinaria compleja ni participar en otras actividades potencialmente peligrosas hasta que se sepa si este medicamento afecta su capacidad para realizar estas actividades.
Interacciones Medicamentosas: Dado que la pregabalina se elimina predominantemente sin cambios en la orina, experimenta un metabolismo insignificante en humanos (<2 % de una dosis recuperada en orina como metabolitos), no inhibe el metabolismo de fármacos in vitro y no se une a proteínas plasmáticas, es poco probable que produzca, o esté sujeta a, interacciones farmacocinéticas. Estudios in vivo y análisis farmacocinético poblacional: En consecuencia, en estudios in vivo no se observaron interacciones farmacocinéticas clínicamente relevantes entre pregabalina y fenitoína, carbamazepina, ácido valproico, lamotrigina, gabapentina, lorazepam, oxicodona o etanol. El análisis farmacocinético poblacional indicó que los antidiabéticos orales, diuréticos, insulina, fenobarbital, tiagabina y topiramato no tuvieron un efecto clínicamente significativo sobre el aclaramiento de pregabalina. Anticonceptivos orales, noretisterona y/o etinilestradiol: La coadministración de pregabalina con anticonceptivos orales como noretisterona y/o etinilestradiol no influye en la farmacocinética en estado estable de ninguna de las sustancias. Productos medicinales que afectan el sistema nervioso central: La pregabalina puede potenciar los efectos del etanol y del lorazepam. En la experiencia poscomercialización, se han reportado casos de insuficiencia respiratoria, coma y muertes en pacientes que toman pregabalina y opioides y/o otros productos medicinales depresores del sistema nervioso central (SNC). La pregabalina parece ser aditiva en el deterioro de la función cognitiva y motora gruesa causada por la oxicodona. Interacciones y los adultos mayores: No se realizaron estudios específicos de interacción farmacodinámica en voluntarios de edad avanzada. Los estudios de interacción solo se han realizado en adultos.
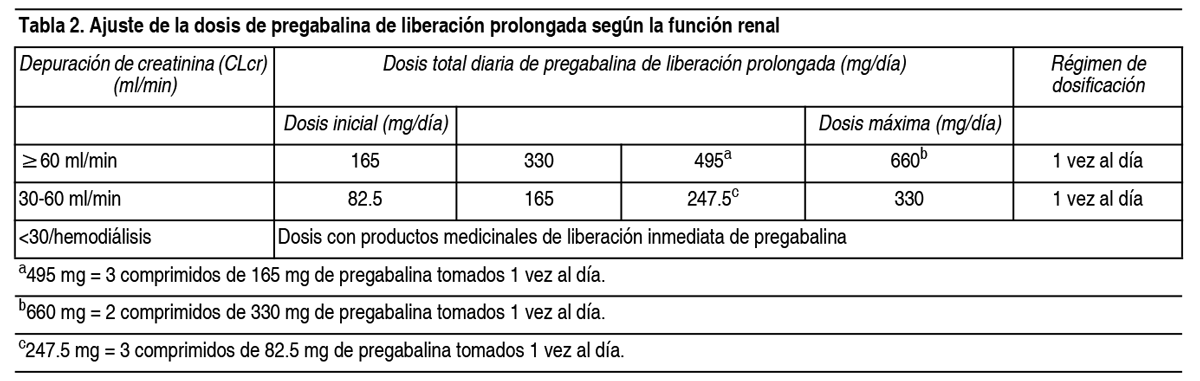
Sobredosificación: En la experiencia poscomercialización, las reacciones adversas más comúnmente reportadas observadas cuando se tomó pregabalina en sobredosis incluyeron somnolencia, estado confusional, agitación e inquietud. También se reportaron convulsiones. En ocasiones raras, se han reportado casos de coma. El tratamiento de la sobredosis de pregabalina debe incluir medidas generales de soporte y puede incluir hemodiálisis si es necesario (Tabla 2).
Conservación: No almacenar por encima de 30 °C.
Presentaciones: Envase conteniendo 30 comprimidos de liberación prolongada. Estuche de cartulina o cartón, debidamente sellado y rotulado, que contiene blísteres de ALU/ALU, rotulado y el folleto de información al paciente. El desecante no debe ser ingerido. No todos los tamańos de envase pueden comercializarse.
 Laboratorio
Laboratorio Laboratorio
Laboratorio Drogas
Drogas Clases Terapéuticas
Clases Terapéuticas Información farmacológica
Información farmacológica

 Ver
Insuficiencia hepática: No se requiere ajuste de dosis para pacientes con deterioro hepático. Población pediátrica: La seguridad y eficacia de la pregabalina en nińos menores de 12 ańos y en adolescentes (de 12 a 17 ańos) no han sido establecidas. Los datos disponibles actualmente se describen en las secciones 4.8 y 5.2, pero no se puede hacer ninguna recomendación sobre la posología. Adultos mayores: Los pacientes ancianos pueden requerir una reducción de dosis de pregabalina debido a una disminución de la función renal. Método de administración: Prexel CR debe tomarse directamente después de una comida nocturna. Prexel CR comprimido debe tragarse entero y no debe partirse, triturarse ni masticarse. El comprimido no debe romperse porque esto podría afectar las características de liberación prolongada. Prexel CR es solo para uso oral.
Ver
Insuficiencia hepática: No se requiere ajuste de dosis para pacientes con deterioro hepático. Población pediátrica: La seguridad y eficacia de la pregabalina en nińos menores de 12 ańos y en adolescentes (de 12 a 17 ańos) no han sido establecidas. Los datos disponibles actualmente se describen en las secciones 4.8 y 5.2, pero no se puede hacer ninguna recomendación sobre la posología. Adultos mayores: Los pacientes ancianos pueden requerir una reducción de dosis de pregabalina debido a una disminución de la función renal. Método de administración: Prexel CR debe tomarse directamente después de una comida nocturna. Prexel CR comprimido debe tragarse entero y no debe partirse, triturarse ni masticarse. El comprimido no debe romperse porque esto podría afectar las características de liberación prolongada. Prexel CR es solo para uso oral.